Update 03.01.2011: RICHTIGSTELLUNG
Die ohne Quellenangabe oder Prüfung vom 17.12.2010 bis 30.12.2010 an dieser Stelle von uns getroffene Behauptung, der Bayerische Apothekerverband habe bewirkt, dass Ampyra ohne Zulassung nicht mehr an Multiple Sklerose-Erkrankte abgegeben werden dürfe, widerrufen wir hiermit (siehe auch Update vom 30.12.2010 direkt untenstehend) als unrichtig.
Gleichzeitig erklären wir, dass deshalb selbstverständlich auch der Hinweis auf die BAV-Website als geeignetes Ziel für Netz-Attacken ("Ionenkanone") ausdrücklich -- und mit großem Bedauern -- zurückgenommen wird.
Anmerkung: Dieser leichtsinnige Cyberattacken-Hinweis war, wie auch bereits am 30.12.2010 hier an dieser Stelle klar erklärt, polemisch und satirisch gemeint und zu keinem Zeitpunkt als ernst gemeinte Aufforderung zu verstehen. Es tut uns aufrichtig leid, wenn dies von unseren Usern ernst gemeint interpretiert wurde.) Gleichzeitig schließen wir die Kommentarfunktion für diesen Beitrag.
Update 30.12.2010: WIDERRUF
In einer früheren Version dieses Beitrags haben wir unrichtige Behauptungen hinsichtlich der an dieser Veränderung beteiligten Personen/Organisationen getroffen, die wir hiermit durch Entfernen voll umfänglich zurück nehmen. Wir kommen dieser Aufforderung gerne nach, da der MS-Reporter mit diesem Bericht zu keinem Zeitpunkt falsche Tatsachen berichten, sondern nur an einem konkreten Beispiel belegen wollte, wie kompliziert die Mechanismen des deutschen Gesundheitsmarkts sind und wie sehr Betroffene diesen ausgeliefert sein können -- soweit gehend, dass konkret lebenserleichternde Maßnahmen (hier: Ampyra®) wieder zurück genommen werden müssen. Als private Webseite ohne Gewinnerzielungsinteresse geht es uns nur um die Betroffenen, aber nicht darum, irgendjemanden für irgendetwas anzuprangern.
Ampyra® darf vorerst nicht mehr an Multiple-Sklerose-PatientInnen in Deutschland abgegeben werden -- wir haben ja seit Ende Oktober einen
Erfahrungsbericht mit Ampyra laufen. Für diejenigen, die gute Resultate damit erzielten, ist dies
ein herber Rückschlag.
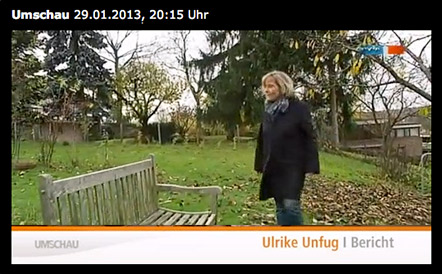




 Dieser Beitrag soll über die nächsten Tage meine Erfahrungen mit der Anwendung von Ampyra® dokumentieren, sowohl hinsichtlich eventueller Nebenwirkungen als auch hinsichtlich der beabsichtigten Wirkung, einer Verbesserung der Gehfähigkeit.
Dieser Beitrag soll über die nächsten Tage meine Erfahrungen mit der Anwendung von Ampyra® dokumentieren, sowohl hinsichtlich eventueller Nebenwirkungen als auch hinsichtlich der beabsichtigten Wirkung, einer Verbesserung der Gehfähigkeit.
 Brigitte-Blog, Blutdrucksenker bei MS und ein US-Amerikaner lässt sich waterboarden.
Brigitte-Blog, Blutdrucksenker bei MS und ein US-Amerikaner lässt sich waterboarden.
 ... ist ein Pharma-unabhängiges Angebot für Multiple Sklerose-Betroffene und ihre Angehörigen. [
... ist ein Pharma-unabhängiges Angebot für Multiple Sklerose-Betroffene und ihre Angehörigen. [